Fermentação e atividade enzimática
Numerosos organismos são capazes de viver na ausência de oxigénio, mobilizando energia dos nutrientes orgânicos por processos fermentativos.
Fermentação
A fermentação é um processo anaeróbio de transformação de uma substância em outra, produzida a partir de microrganismo, tais como bactérias e fungos, chamados nestes casos de fermentos.
Benefícios da Fermentação
- A fermentação melhora a absorção de nutrientes importantes, especialmente ferro e zinco.
- A fermentação melhora o conteúdo proteico e adiciona vitaminas e minerais.
- Muitas pessoas preferem o sabor dos alimentos fermentados. Alguns dizem que o sabor azedo ajuda a recuperar o apetite quando as pessoas estão doentes.
- As acetobactérias provocam o azedamento do vinho e dos sucos e frutas, sendo responsáveis pela produção do vinagre.
- O ácido que é produzido na fermentação azeda ajuda a conservar os alimentos.
Entre vários processos fermentativos salientam-se a fermentação lática, a fermentação alcoólica e a fermentação acética.

Fermentação Lática
A Fermentação Lática consiste na conversão anaeróbica parcial de carboidratos (mais especificamente a glicose) com a produção final de ácido lático, além de várias outras substâncias orgânicas. É um processo de grande importância utilizado pelo homem na produção de laticínios (queijos, manteiga, etc.). Por outro lado, é processo responsável pela deterioração de vários produtos agrícolas.
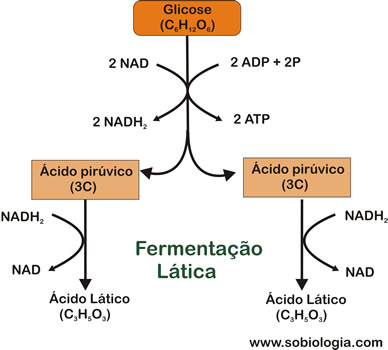
Fermentação lática.
Na fermentação lática intervêm várias bactérias, entre as quais se evidenciam a atividade de lactobactérias pertencentes aos géneros Lactobacillus e Streptococcus. Estas bactérias desencadeiam reações de fermentação no leite, utilizando como substrato diversos açúcares. Após a glicólise, o piruvato experimenta uma redução, originando-se ácido lático.

O iogurte resulta de fermentação lática.
Fermentação Alcoólica
A fermentação alcoólica é um processo anaeróbico no qual açúcares como a glicose, frutose e sacarose são convertidos em energia celular com produção de etanol e dióxido de carbono como resíduos metabólicos. A fermentação alcoólica é essencial na produção de vinho e cerveja.
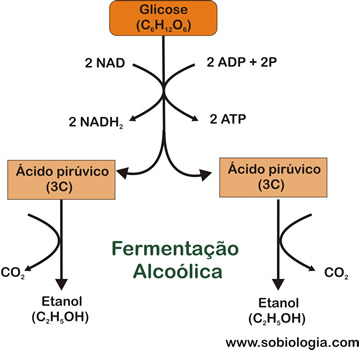
Fermentação alcoólica.
Na fermentação alcoólica, as duas moléculas de ácido pirúvico produzidas são convertidas em álcool etílico (também chamado de etanol), com a liberação de duas moléculas de CO2 e a formação de duas moléculas de ATP.

O vinho é produzido por fermentação alcoólica.
O vinho deixado em contato com o ar pode produzir vinagre, um produto rico em ácido acético.
Fermentação Acética
A fermentação acética consiste na oxidação parcial do álcool etílico, com produção de ácido acético. Este processo é utilizado na produção de vinagre comum e do ácido acético industrial. Desenvolve-se também na deterioração de bebidas de baixo teor alcoólico e na de certos alimentos. É realizada por bactérias denominadas acetobactérias, produzindo ácido acético e dióxido de carbono.
Enzimas em ação
As enzimas são substâncias orgânicas que catalisam reações bioquímicas, controlando a sua velocidade.
Os catalisadores caraterizam-se por:
- baixarem a energia de ativação necessária para que ocorram as reações químicas que catalisam;
- não alterarem o equilíbrio químico das reações em que participam;
- não serem destruídos pelo efeito da reação.
Algumas propriedades das Enzimas:
- são catalisadores biológicos extremamente eficientes e aceleram em média 109 a 1012 vezes a velocidade da reação;
- são específicas;
- não são destruídas pelo efeito da reação, podendo ser usadas de novo;
- atuam em concentrações muito baixas e em condições suaves de temperatura e pH.
- são destruídas por temperaturas elevadas. As baixas temperaturas inibem a sua ação, voltando a atuar quando as condições do meio são adequadas.
Estrutura das enzimas – Interação Enzima – Substrato
As enzimas, em regra, têm maiores dimensões que os substratos sobre os quais atuam. A ligação entre as duas moléculas que formam o complexo enzima-substrato faz-se na zona do centro ativo.

Interação enzima-substrato.
Como observamos no gráfico anterior, na interação enzima substrato há, inicialmente, uma grande concentração de substrato relativamente à de enzima livre. As moléculas do substrato vão ligar-se a moléculas enzimáticas, formando complexos enzima-substrato (ES). Assim, enquanto as concentrações de substrato (S) e de enzima livre (E) diminuem, a concentração do complexo enzima-substrato vai aumentando. À medida qua as moléculas enzimáticas catalisam a reação, vão-se constituindo moléculas de produto (P), verificando-se que a concentração no meio vai aumentando.
As ligações que se estabelecem entre a enzima e o substrato são transitórias. Ao terminar a reação libertam-se os produtos formados, ficando a enzima livre. A molécula enzimática pode então atuar sobre outra molécula de substrato, repetindo-se o ciclo até que todo o substrato esteja transformado.
Deste modo, uma pequena quantidade de enzima pode catalisar uma grande quantidade de substrato.

